細胞の由来動物種を同定する検査です。旭硝子社製のオーセンティキットを使用します。(現在は販売中止)
細胞の抽出液を電気泳動し、電気泳動後に目的の酵素を酵素基質液と反応させて発色させます。電気泳動の移動度が動物種により異なることを利用して、由来動物種を特定します。
酵素基質LD(Lactate Dehydrogenase)とNP(Purine nucleoside phosphorylase)をルーチンに使用しています。
※現在は、Isozyme検査の代わりに動物種PCR検査を行っています。
1. 準備するもの
(1) 検体
- 検査検体(細胞ペレット)
- 陽性対照1:HeLa S-3 抽出物(旭テクノグラス社, #61-039-039)
- 陽性対照2:L929 抽出物(旭テクノグラス社, #61-039-037)
(2) 試薬
- Cell Extraction Buffer (旭テクノグラス社, # 61-039-030)
- Enzyme Stabilizer (旭テクノグラス社, #61-039-032)
- ユニバーサルゲル/8(ヘレナ研究所, #470100)
- ユニバーサルバッファー(ヘレナ研究所, #470180)
- 酵素基質 LD(旭テクノグラス社, #61-039-014)
- 酵素基質 NP(旭テクノグラス社, #61-039-002)
- 酵素基質 PepB(旭テクノグラス社, #61-039-010)
- 酵素基質 AST(旭テクノグラス社, #61-039-012)
- 酵素基質 MPI(旭テクノグラス社, #61-039-008)
- 酵素基質 G6PD(旭テクノグラス社, #61-039-004)
- 酵素安定用バッファー(旭テクノグラス コード番号:R-578)
(3) 容器
- オーセンティキット専用電気泳動装置(旭テクノグラス)
- パワーサプライ
- インキュベータトレイ
2. 方法
(1) 検体の調製
検体の調製は氷上で行う。
- 細胞(約2×106個)を回収する(ペレットの状態で50μl以上が望ましい)。
- PBS(-)で2回遠心洗浄した後、洗浄液を捨てる。(細胞ペレット)
- 細胞ペレットと等量のCell Extraction Buffer(10~100μl程度)を加え、ピペッティングによりペレットを完全に懸濁する。
- 15分間氷上に静置する。
- ミキサーに2、3回軽く押し当てるようにして攪拌する。
- 15000rpm、4℃、5分間遠心する。
- 上清を新しい微量遠心チューブに移す。これを泳動用サンプルとする。
- 凍結保存する場合は、上清と同量の酵素安定用バッファーを加え、-20℃に凍結保存する。
(2) 電気泳動
- 専用電気泳動装置のカバーを氷水で満たす。
- ゲルのウェルに、サンプルとコントロールとなるL929 抽出物、HeLa S-3 抽出物を0.8μlずつアプライする。
- 4℃に冷却したユニバーサルバッファーを専用電気泳動装置に入れ、ゲルをセットする。
- 90V、60分間電気泳動する。
(3) 染色
- 酵素基質を500μlのユニバーサルバッファーに溶解する。
- 微量遠心チューブに移し、軽く遠心して不溶物を沈降させる。
- 泳動後のゲルを泳動槽カバーからはずす。
- ゲルの+極側に溶解した酵素基質をのせる。
- 酵素基質液をゲル上に均一に塗り広げる。
- インキュベータトレイに超純水で湿らせたキムワイプを敷き、その上にゲルを乗せて蓋をする。
- 37℃で発色の様子を観察しながら、10~30分間程度反応させる。
- バンドが現れたら、超純水を入れたバットにゲルを浸して15分間程度振盪機で軽く振り、余分な酵素を除く。
- 超純水を新しいものに交換し、さらに15分間程度振盪する。
- ゲルを一晩室温で乾燥させる。
結果例
| 酵素基質LD | 酵素基質NP |
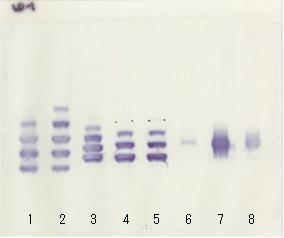 |
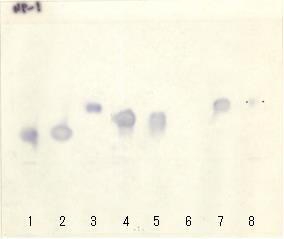 |
1. HeLa.S3抽出物 (ヒト)(陽性対照1) 2. ヒト 3. ウサギ 4. ミンク 5. ミンク 6. マウス 7. マウス 8. L929抽出物(マウス)(陽性対照2)
3. 判定
各レーンのバンドが、コントロールとなるL929(Mouse)及びHeLa S3(Human)のバンド位置と比較して相対的に正しい位置に出ているか、バンドパターン図と照合し確認する。
動物種による移動度(バンドパターン図)例
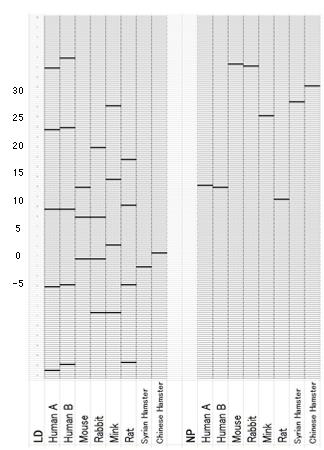
・バンドパターン図文献
The AuthentiKit System Handbook For Cell Authentication And Identification (Innovative Chemistry)
JCRB NEWSLETTER別冊p30 1985 Oct
In vitro 16(2) 119-135 1980 PubMed ID : 6988327
・バンドパターン図に記載の動物種
酵素基質LD、NP、G6PD、PepB、MPI、AST:human、mouse、rat、dog、monkey(cercopithecus)、monkey(rhesus)、fox、horse、cat、guinea pig、hamster(syrian)、hamster(chinese)、bovine、rabbit、aoudad、raccoon、baboon、bat、buffalo、mink
酵素基質LD、NP、G6PD:cattle
酵素基質NP、PepB、MPI:marmoset、goat、pig(G6PDも可)、sheep




